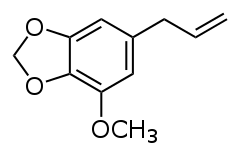
Mirystycyna
Mirystycyna – organiczny związek chemiczny o działaniu psychoaktywnym[2] występujący w olejku eterycznym gałki muszkatołowej. Cząsteczka mirystycyny zbudowana jest z dwupierścieniowego szkieletu 1,3-benzodioksolu zawierającego podstawnik metoksylowy (–OCH3) i allilowy (–CH2–CH=CH2).
| ||||||||||||||||||||||||||||||||||||||||||

| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C11H12O3 | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
192,21 g/mol | |||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwna, oleista ciecz[1] | |||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||
Aktywność biologiczna edytuj
Jest naturalnym insektycydem, prawdopodobnie wykazuje też działanie neurotoksyczne na komórki rakowe nerwiaka płodowego[5]. Jest słabym inhibitorem monoaminooksydazy[6].
Wbrew dawnym przypuszczeniom, mirystycyna nie jest metabolizowana do pochodnych amfetaminy; stwierdzono natomiast, że ulega ona demetylenacji i następczej metylacji[7].
Działanie psychoaktywne ujawnia się po spożyciu znacznie większych ilości substancji, niż jest obecna w gałce muszkatołowej stosowanej jako przyprawa kuchenna. Działanie to nie przypomina ani MDMA, ani psychodelików, jednak efekty są podobne do tych, jakie pojawiają się po zażyciu marihuany, na przykład suchość ust, euforia, wzmożona wesołość. W dużych dawkach powoduje zaburzenia świadomości i percepcji, efekty wizualne, omdlenia, długotrwałą senność i zmęczenie w wyniku silnego obniżenia ciśnienia krwi[potrzebny przypis]. Efekty psychoaktywne, po spożyciu sproszkowanej gałki muszkatołowej, pojawiają się po 2–7 h i trwają do 24 h, a niektóre efekty drugorzędowe do 72 h[8].
Mirystycyna może być używana jako półprodukt do syntezy MMDA, w reakcji podobnej do otrzymywania MDMA z safrolu[potrzebny przypis].
Przypisy edytuj
- ↑ a b c d e f g Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b A.T. Shulgin. Possible implication of myristicin as a psychotropic substance. „Nature”. 210 (5034), s. 380-384, 1966. DOI: 10.1038/210380a0. PMID: 5336379.
- ↑ a b Mirystycyna (nr 09237) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski.
- ↑ ChemIDplus: Myristicin
- ↑ Lee BK, Kim JH, Jung JW, Choi JW, Han ES, Lee SH, Ko KH, Ryu JH. Myristicin-induced neurotoxicity in human neuroblastoma SK-N-SH cells. „Toxicol. Lett.”. 157 (1), s. 49–56, 2005. DOI: 10.1016/j.toxlet.2005.01.012. PMID: 15795093.
- ↑ Truitt EB, Duritz G, Ebersberger EM. Evidence of monoamine oxidase inhibition by myristicin and nutmeg. „Proc. Soc. Exp. Biol. Med.”. 112, s. 647–650, 1963. PMID: 13994372.
- ↑ J. Beyer, D. Ehlers, HH. Maurer. Abuse of nutmeg (Myristica fragrans Houtt.): studies on the metabolism and the toxicologic detection of its ingredients elemicin, myristicin, and safrole in rat and human urine using gas chromatography/mass spectrometry.. „Ther Drug Monit”. 28 (4), s. 568-75, 2006. PMID: 16885726.
- ↑ Nutmeg: Basics. Erowid. [dostęp 2011-08-12].