Szczepionka BCG
BCG (od Bacillus Calmette-Guérin) – szczepionka opracowana we Francji w 1921 roku przez Alberta Calmette'a i Camille'a Guérina i stosowana przede wszystkim przeciw gruźlicy. Szczepionka zawiera atenuowany, ale żywy szczep bakterii Mycobacterium bovis (gatunek pokrewny, wywołujący gruźlicę bydła). Atenuację uzyskuje się wskutek 231 pasaży na podłożu z żółcią. Szczepienia okazały się skuteczne w Europie i krajach rozwijających się. Próby z tą szczepionką w USA wykazały niewielkie właściwości ochronne (odmienny szczep Mycobacterium tuberculosis), w pozostałych krajach zaobserwowano zróżnicowaną skuteczność. Obecnie stosowana w Europie, nieużywana w USA.
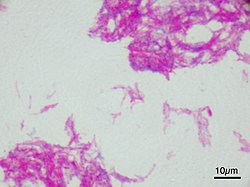
W krajach, gdzie występuje trąd, stosuje się szczepionkę BCG u zdrowych dzieci, wkrótce po urodzeniu[1].
Historia edytuj
Badania nad szczepionką na gruźlicę, które finalnie doprowadziły do powstania BCG, rozpoczęto w 1900 roku, w Instytucie Pasteura w Lille. Na czele projektu postawiono dwóch naukowców - Alberta Calmette i Camille'a Guérin. Pierwsze testy na zwierzętach zaplanowane zostały w 1913 roku, jednak ich przeprowadzenie uniemożliwił wybuch I Wojny Światowej i okupacja Lille przez wojska niemieckie. W 1919 roku udowodniono już niewywoływanie objawów gruźlicy przez wyhodowane szczepy na wielu gatunkach zwierząt, stąd 18 czerwca 1921 po raz pierwszy podano BCG człowiekowi w Szpitalu Charité w Paryżu. Do końca 1924 roku zaszczepiono 664 noworodki, a w latach 1924-1928 - 114 tysięcy. W 1928 roku Liga Narodów swoim autorytetem potwierdziła bezpieczeństwo zastosowania szczepionki BCG[2][3].
W 1930 roku w niemieckiej Lubece wskutek modyfikacji schematu użycia szczepionki przez miejscowych lekarzy, doszło do śmierci 73 noworodków, a 135 innych rozwinęło objawy gruźlicy, z której jednak zostały one wyleczone. Wydarzenie to przeszło do historii jako "Tragedia w Lubece". Specjalny raport przygotowany przez komisję powołaną przez niemiecki rząd za całe zajście obwinił szczepionkę i jej twórców. Zarzuty te jednak nie zostały potwierdzone, a sam Calmette wybronił się w zeznaniach przed Międzynarodową Unią ds. Walki z Gruźlicą (dostał nawet owacje na stojąco). Incydent mimo to doprowadził do podkopania autorytetu szczepionki[2].
Zastosowanie medyczne szczepionki BCG zapoczątkowano 1921 roku i w 1977 znalazła się na liście leków podstawowych Światowej Organizacji Zdrowia[4]. Szczepionkę podaje się rocznie (2004) około 100 milionom dzieci na całym świecie[5].
Stosowanie w Polsce edytuj
W Polsce szczepienia przy użyciu BCG rozpoczęto w 1926 r., głównie w Poznaniu, Warszawie i Wilnie. Produkcję szczepionki powierzono Państwowemu Zakładowi Higieny, zaś organizację szczepień Polskiemu Związkowi Przeciwgruźliczemu. Do 1939 roku w Polsce zaszczepiono 70 tysięcy osób. W 1945 roku wznowiono produkcję i akcję szczepień, a na mocy porozumienia z Duńskim Czerwonym Krzyżem z 1947 roku, rozpoczęto masowe szczepienia. W latach 1947-1950 śródskórnie zaszczepiono 4,5 miliona dzieci i młodzieży od 1 do 18 roku życia. Od 1951 roku BCG jest w Polsce szczepieniem obowiązkowym[6].
Inne zastosowania edytuj
Inne choroby zakaźne edytuj
BCG ma około 26% działania ochronnego przeciw trądowi[7], chociaż szczepionka nie jest wykorzystywana w tym celu. Potencjalnie zmniejsza ryzyko infekcji gronkowcowych, kandydozy, grypy i żółtej febry[8].
BCG a COVID-19 edytuj
Pierwotnie raportowana była mniejsza częstość zachorowań na COVID-19 w krajach o wysokim poziomie wyszczepialności przy pomocy szczepionki BCG[8], jednak obecnie dominującą tezą jest, że jest to przypadkowa zależność u podłoża której leżą inne czynniki (np. mniejszy poziom urbanizacji państw dawnego Bloku Wschodniego)[9]. Mimo to jednak w modelach bioinformatycznych oraz w części badań na zwierzętach taki wpływ protekcyjny oparty o mechanizm odporności krzyżowej, został potwierdzony[10][11][12]. Pierwsze wyniki randomizowanej próby klinicznej z Malawi nie potwierdziły protekcyjnego efektu BCG na przebieg COVID-19[13]. Część naukowców wystosowała hipotezę, jakoby rozbieżności w wynikach danych eksperymentalnych i klinicznych wynikała ze stosowania różnych szczepów szczepionki BCG w różnych krajach[14].
Nowotwory edytuj
BCG jest przydatna w leczeniu powierzchownych postaci raka pęcherza moczowego. Od końca lat 1980. pojawiały się dowody na to, że zakroplenie BCG do pęcherza jest skuteczną formą immunoterapii w tej chorobie[15]. Podczas gdy mechanizm jest niejasny, wydaje się, że przeciwko guzowi zostaje uruchomiona lokalna reakcja immunologiczna. Immunoterapia przy użyciu BCG zapobiega nawrotom w ⅔ przypadków powierzchownych nowotworów pęcherza moczowego. BCG jest także do wykorzystania w immunoterapii raka okrężnicy[16] oraz w leczeniu sarkoidozy u koni.
Cukrzyca edytuj
W badaniach klinicznych w oparciu o prace Denise'a Faustmana wykorzystano BCG do pobudzenia produkcji TNF-α, który może zabić limfocyty T odpowiedzialne za cukrzycę typu 1. W badaniach na myszach wykazano, że zastosowanie podobnego leczenia daje całkowite wyleczenie u jednej trzeciej badanych myszy[17]. 8 sierpnia 2012 Denise Faustman opublikowała wyniki badań etapu I polegającego na sprawdzeniu wyników badań na myszach do tego, jak dawki szczepionki BCG działają na ludzi. U większości przypadków odnotowano pozytywną zmianę, czyli zmniejszenie się liczby limfocytów zabijających komórki produkujące insulinę. Aktualnie zbierane są środki na rozpoczęcie kolejnej fazy badań.
Niepożądane odczyny poszczepienne edytuj
Poważne odczyny poszczepienne są rzadkie. Najczęściej w miejscu wstrzyknięcia występuje zaczerwienienie, obrzęk i bolesność. Czasem może powstać małe owrzodzenie z wytworzeniem blizny po wygojeniu. O wiele częściej odczyny poszczepienne występują i mają cięższy przebieg, do zagrożenia życia włącznie, u osób z zaburzeniami odporności. U tych osób i w czasie ciąży szczepionka BCG jest przeciwwskazana. Odmiennie niż większość szczepionek, szczepionka ta zawiera atenuowane, ale żywe bakterie Mycobacterium bovis, co może w stanach osłabionej odporności organizmu wywołać groźną, pełnoobjawową chorobę.
Przypisy edytuj
- ↑ World Health Organization, BCG vaccines: WHO position paper – February 2018, „Weekly Epidemiological Record”, 93 (08), 23 lutego 2018, s. 73–96 [dostęp 2021-01-03] (ang.).
- ↑ a b Simona Luca, Traian Mihaescu, History of BCG Vaccine, „Maedica”, 8 (1), 2013, s. 53–58, ISSN 1841-9038, PMID: 24023600, PMCID: PMC3749764 [dostęp 2022-09-01].
- ↑ Niyati Lobo i inni, 100 years of Bacillus Calmette-Guérin immunotherapy: from cattle to COVID-19, „Nature Reviews. Urology”, 18 (10), 2021, s. 611–622, DOI: 10.1038/s41585-021-00481-1, ISSN 1759-4820, PMID: 34131332, PMCID: PMC8204595 [dostęp 2022-09-01].
- ↑ World Health Organization, World Health Organization model list of essential medicines: 21st list 2019 [online], 2019 [dostęp 2021-01-03] (ang.).
- ↑ World Health Organization, Weekly epidemiological record, 2004
- ↑ Zygmunt Moskwa, Historia szczepień przeciwgruźliczych i powstanie szczepionki BCG, „Wiadomości Lekarskie”, 36 (1), 1983, s. 81-85 (pol.).
- ↑ Black GF., Weir RE., Floyd S., Bliss L., Warndorff DK., Crampin AC., Ngwira B., Sichali L., Nazareth B., Blackwell JM., Branson K., Chaguluka SD., Donovan L., Jarman E., King E., Fine PE., Dockrell HM. BCG-induced increase in interferon-gamma response to mycobacterial antigens and efficacy of BCG vaccination in Malawi and the UK: two randomised controlled studies.. „Lancet”. Apr 20;359. 9315, s. 1393-401, 2002. DOI: 10.1016/S0140-6736(02)08353-8. PMID: 11978337.
- ↑ a b Paul K. Hegarty i inni, COVID-19 and Bacillus Calmette-Guérin: What is the Link?, „European Urology Oncology”, 3 (3), 2020, s. 259–261, DOI: 10.1016/j.euo.2020.04.001, ISSN 2588-9311, PMID: 32327396, PMCID: PMC7152883 [dostęp 2020-10-09].
- ↑ Matteo Riccò i inni, Stop playing with data: there is no sound evidence that Bacille Calmette-Guérin may avoid SARS-CoV-2 infection (for now)., „Acta Bio Medica Atenei Parmensis”, 91 (2), 2020, s. 207–213, DOI: 10.23750/abm.v91i2.9700, PMID: 32420947, PMCID: PMC7569626 [dostęp 2022-09-01].
- ↑ Yusuke Tomita i inni, BCG vaccine may generate cross-reactive T cells against SARS-CoV-2: In silico analyses and a hypothesis, „Vaccine”, 38 (41), 2020, s. 6352–6356, DOI: 10.1016/j.vaccine.2020.08.045, ISSN 0264-410X, PMID: 32863070, PMCID: PMC7440160 [dostęp 2022-09-01] (ang.).
- ↑ Sanja Glisic i inni, Biological Rationale for the Repurposing of BCG Vaccine against SARS-CoV-2, „Journal of Proteome Research”, 19 (11), 2020, s. 4649–4654, DOI: 10.1021/acs.jproteome.0c00410, ISSN 1535-3907, PMID: 32794723 [dostęp 2022-09-01].
- ↑ Nadia Rahali, Chokri Bahloul, Induction of Cross-Reacting Antibodies Against the COVID-19 by BCG Vaccination in the Mouse Model, „Current Microbiology”, 79 (9), 2022, s. 275, DOI: 10.1007/s00284-022-02971-w, ISSN 1432-0991, PMID: 35907089, PMCID: PMC9362411 [dostęp 2022-09-01].
- ↑ Judith R. Glynn i inni, The effect of BCG revaccination on all-cause mortality beyond infancy: 30-year follow-up of a population-based, double-blind, randomised placebo-controlled trial in Malawi, „The Lancet Infectious Diseases”, 21 (11), 2021, s. 1590–1597, DOI: 10.1016/S1473-3099(20)30994-4, ISSN 1473-3099, PMID: 34237262, PMCID: PMC8550897 [dostęp 2022-09-01] (ang.).
- ↑ Masayuki Miyasaka, Is BCG vaccination causally related to reduced COVID-19 mortality?, „EMBO molecular medicine”, 12 (6), 2020, e12661, DOI: 10.15252/emmm.202012661, ISSN 1757-4684, PMID: 32379923, PMCID: PMC7267326 [dostęp 2022-09-01].
- ↑ Lamm DL., Blumenstein BA., Crawford ED., Montie JE., Scardino P., Grossman HB., Stanisic TH., Smith JA., Sullivan J., Sarosdy MF. A randomized trial of intravesical doxorubicin and immunotherapy with bacille Calmette-Guérin for transitional-cell carcinoma of the bladder.. „N Engl J Med”. Oct 24;325. 17, s. 1205-9, 1991. PMID: 1922207.
- ↑ Mosolits S., Nilsson B., Mellstedt H. Towards therapeutic vaccines for colorectal carcinoma: a review of clinical trials.. „Expert Rev Vaccines”. Jun;4. 3, s. 329-50, 2005. DOI: 10.1586/14760584.4.3.329. PMID: 16026248.
- ↑ Human trials to begin on 'diabetes cure' after terminally ill mice are returned to health | Mail Online