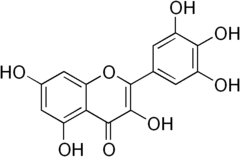
Mirycetyna
Mirycetyna – organiczny związek chemiczny z grupy flawonoli, będących flawonoidami, które występuje naturalnie wielu w owocach, winogronach, warzywach, ziołach i innych roślinach. Orzech włoski należy do jednego z bogatszych źródeł tego flawonoidu. Jest jednym ze związków fenolowych obecnych w czerwonym winie[3].
| |||||||||||||||||||
| |||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||
| Wzór sumaryczny |
C15H10O8 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
318,23 g/mol | ||||||||||||||||||
| Identyfikacja | |||||||||||||||||||
| Numer CAS | |||||||||||||||||||
| PubChem | |||||||||||||||||||
| DrugBank | |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||
Właściwości
edytujMirycetyna posiada właściwości przeciwutleniające. Badania in vitro sugerują, że w wysokich stężeniach może zmieniać LDL cholesterolu, powodując wzrost jego absorpcji przez białe krwinki.
Fińskie badania wiążą wysokie spożycie mirycetyny z obniżonym ryzykiem zachorowania na raka prostaty[4].
Inne, 8-letnie badania wykazały, że trzy flawonole – kemferol, kwercetyna i mirycetyna – obniżyły ryzyko zachorowania na raka trzustki o 23%[5].
Metabolizm
edytuj- Mirycytryna jest ramnozydem mirycetyny,
- 3-O-rutynozyd mirycetyny
- O-Metylopochodne
- Larycytryna jest tworzona z mirycetyny w wyniku działania enzymu O-metylotransferazy mirycetyny[6].
Przypisy
edytuj- ↑ Myricetin, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2021-05-28] (ang.).
- ↑ Myricetin (nr M6760) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2011-07-01]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ M. Maggiolini i inni, The red wine phenolics piceatannol and myricetin act as agonists for estrogen receptor alpha in human breast cancer cells, „Journal of Molecular Endocrinology”, 35, 2005, s. 269–281, DOI: 10.1677/jme.1.01783 (ang.).
- ↑ P. Knekt i inni, Flavonoid intake and risk of chronic diseases, „American Journal of Clinical Nutrition”, 76 (3), 2002, s. 560–568, DOI: 10.1093/ajcn/76.3.560, PMID: 12198000 (ang.).
- ↑ U. Nöthlings i inni, Flavonols and pancreatic cancer risk: the multiethnic cohort study, „American Journal of Epidemiology”, 166 (8), 2007, s. 924–931, DOI: 10.1093/aje/kwm172, PMID: 17690219 (ang.).
- ↑ H. Foerster, MetaCyc Pathway: syringetin biosynthesis [online], 3 listopada 2006 [dostęp 2011-01-07] (ang.).
Linki zewnętrzne
edytuj- Aktywność biologiczna flawonoidów [online] (pol.).