Glukoza
Glukoza, D-glukoza[a] – organiczny związek chemiczny, monosacharyd (cukier prosty) z grupy aldoheksoz. Jest białym, drobnokrystalicznym ciałem stałym[2], z roztworów wodnych łatwo krystalizuje jako monohydrat[8]. Jest bardzo dobrze rozpuszczalna w wodzie[2] (nie zmienia pH roztworu). Ma słodki smak, nieco mniej intensywny od sacharozy[9].
| |||||||||||||||||||||
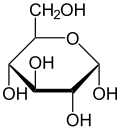
 α-D-glukopiranoza (projekcja stereochemiczna) | |||||||||||||||||||||
| |||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||
| Wzór sumaryczny |
C6H12O6 | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
180,16 g/mol | ||||||||||||||||||||
| Wygląd |
bezwonne[1], bezbarwne, drobne kryształki o słodkim smaku[2] | ||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||
| Numer CAS |
50-99-7 | ||||||||||||||||||||
| PubChem | |||||||||||||||||||||
| DrugBank | |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||
| Pochodne | |||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||||||||
| ATC | |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
Enancjomerem D-glukozy jest L-glukoza, niewystępująca w organizmach wyższych.
Występowanie edytuj
Glukoza powstaje w organizmach roślinnych podczas fotosyntezy[10]:
Występuje w znacznych ilościach w owocach (szczególnie w winogronach, stąd nazywana jest czasem cukrem gronowym) i miodzie. W organizmach jest składowana w postaci dwóch polimerów: skrobi u roślin i glikogenu u zwierząt[11].
Budowa cząsteczki edytuj
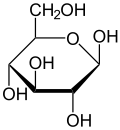
Krystaliczna glukoza ma budowę cykliczną. Sześcioczłonowy pierścień hemiacetalu powstaje w wyniku reakcji grupy aldehydowej przy atomie węgla C1 z grupą hydroksylową przy atomie węgla C5 w łańcuchu. Możliwe są zatem dwa anomery – α oraz β w zależności od położenia grupy OH przy pierwszym atomie węgla formy cyklicznej.
W roztworze wodnym oba anomery mogą ulegać reakcji otwarcia pierścienia i ponownego zamknięcia z utworzeniem ponownie takiego samego lub przeciwnego anomeru. Proces taki nazywa się mutarotacją. Forma otwartołańcuchowa występuje wyłącznie w roztworze wodnym, a jej termodynamiczna stabilność jest znacznie mniejsza od formy cyklicznej, dlatego równowaga procesu mutarotacji przesunięta jest silnie w kierunku formy cyklicznej, która występuje w przewadze.
W łańcuchowej formie glukozy znajdują się cztery asymetryczne atomy węgla (tj. C2, C3, C4 i C5), podczas gdy w formie cyklicznej występuje pięć takich atomów (dodatkowo asymetryczny jest węgiel anomeryczny, C1). W zależności od położenia grupy karbonylowej w łańcuchu i konfiguracji asymetrycznych atomów węgla, możliwych jest kilkadziesiąt izomerów glukozy (zob. heksozy). Jednym z często występujących naturalnie izomerów glukozy jest fruktoza, różniąca się położeniem grupy karbonylowej.
Właściwości edytuj
Właściwości chemiczne edytuj
Naturalna glukoza jest jednym z wielu izomerów optycznych tego związku – α-D-glukopiranozą (dekstrozą). Jest ona czynna optycznie – w temperaturze pokojowej skręca płaszczyznę spolaryzowanego światła białego w prawo. Skręcalność właściwa anomeru α wynosi +112°, natomiast anomeru β +19°. W roztworze wodnym w wyniku mutarotacji ustala się stan równowagi obu anomerów w stosunku 36:64, o skręcalności właściwej +52,6°[12].
Glukoza w przeciwieństwie do fruktozy odbarwia wodę bromową w obecności kwaśnego węglanu sodu[13] (następuje utlenienie grupy aldehydowej do grupy karboksylowej, w wyniku czego powstaje kwas glukonowy)[2]:
- CH
2OH−(CHOH)
4−CHO + Br
2 + 2NaHCO
3 → CH
2OH−(CHOH)
4−COOH + 2NaBr + H
2O + 2CO
2↑
Pod wpływem kwasu azotowego grupa aldehydowa oraz atom węgla C6 są utleniane do grup karboksylowych, w wyniku czego powstaje kwas glukarowy (który w gorącej wodzie przechodzi w lakton)[2].
W temperaturze powyżej 150 °C topi się i brunatnieje, tworząc (podobnie jak sacharoza) karmel[2].
Właściwości biologiczne edytuj
D-Glukoza jest podstawowym związkiem energetycznym dla większości organizmów, przechowywanym pod postacią polimerów – skrobi i glikogenu. Stanowi cukier najłatwiej przyswajalny przez człowieka[2]. W procesie glikolizy jest rozkładana na kwas pirogronowy. Jest także substratem wielu procesów zachodzących w komórce, a u roślin, jako celuloza, podstawowym budulcem ściany komórkowej.
Wykrywanie glukozy w roztworach edytuj
| Ta sekcja od 2011-10 wymaga zweryfikowania podanych informacji. |
Glukozę, podobnie jak inne cukry redukujące, można wykryć m.in. za pomocą prób Trommera i Tollensa[2]. W obydwu próbach glukoza jest przeprowadzana w kwas glukonowy.
Próba Trommera edytuj
Do świeżo strąconego osadu wodorotlenku miedzi(II) dodaje się badany roztwór i ogrzewa. W obecności glukozy niebieski osad Cu(OH)2 zmienia barwę na ceglastoczerwoną, wskutek redukcji do Cu
2O:
- 2Cu(OH)
2 + C
6H
12O
6 → Cu
2O + C
6H
12O
7 + 2H
2O
Próba Tollensa edytuj
Do probówki napełnionej niewielką ilością roztworu azotanu srebra należy dodać kilka kropli stężonego roztworu wodorotlenku sodu (NaOH), a następnie dolewać kroplami roztworu amoniaku (NH
3), aż do rozpuszczenia się powstałego wcześniej osadu.
- 1. AgNO
3 + NaOH → AgOH + NaNO
3 - 2a. 2AgOH → Ag
2O + H
2O - 2b. Ag
2O + CH
2(OH)(CHOH)
4CHO → 2 Ag + CH
2(OH)(CHOH)
4COOH
Tak przygotowaną probówkę należy umieścić w zlewce z gorącą wodą (na łaźni wodnej). Na koniec do probówki dodaje się badany roztwór. Podczas ogrzewania substancji o barwie brunatnej – Ag
2O (powstałej z reakcji AgNO
3 z NaOH) – na ściankach probówki osadza się warstewka metalicznego srebra – lustro srebrowe (z tej przyczyny próba Tollensa zwana jest także próbą lustra srebrnego).
- 3. Ag
2O + glukoza → 2 Ag + kwas organiczny (kwas glukonowy) - Ag
2O + C
6H
12O
6 → 2 Ag + C
6H
12O
7
Zastosowanie edytuj
W medycynie (np. kroplówki), a także w przemyśle spożywczym (np. syrop glukozowy[14], syrop glukozowo-fruktozowy) oraz farmaceutycznym[2]. Stosowana jest również jako dodatek o właściwościach nawilżających do kosmetyków[15][16], np. przeznaczonych do makijażu, pielęgnacji skóry i włosów[15].
Uwagi edytuj
Przypisy edytuj
- ↑ Glucose, [w:] GESTIS-Stoffdatenbank, Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, ZVG: 019010 [dostęp 2022-07-23] (niem. • ang.).
- ↑ a b c d e f g h i Podręczny słownik chemiczny, Romuald Hassa (red.), Janusz Mrzigod (red.), Janusz Nowakowski (red.), Katowice: Videograf II, 2004, s. 150–151, ISBN 83-7183-240-0.
- ↑ a b c d Haynes 2016 ↓, s. 3-282.
- ↑ a b Farmakopea Polska VIII, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2008, s. 3491, ISBN 978-83-88157-53-0.
- ↑ Haynes 2016 ↓, s. 5-92.
- ↑ a b c Haynes 2016 ↓, s. 5-152.
- ↑ D-(+)-Glucose, karta charakterystyki produktu Sigma-Aldrich, Merck, 21 stycznia 2021, numer katalogowy: G8270 [dostęp 2023-07-09]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ R.C.G. Killean, W.G. Ferrier, D.W. Young, A preliminary investigation of the crystal and molecular structure of α-D-glucose monohydrate, „Acta Crystallographica”, 15 (9), 1962, s. 911–912, DOI: 10.1107/S0365110X62002352 (ang.).
- ↑ Learning, Food Resource [online], Oregon State University [zarchiwizowane z adresu 2015-01-09].
- ↑ Theodore Brown, John D. Nelson, Kenneth W. Kemp, Chemistry. The Central Science, Upper Saddle River: Prentice Hall, 2003, s. 958, ISBN 0-13-048450-4.
- ↑ Marzena Popielarska, Robert Konieczny, Grzegorz Góralski, Słownik szkolny. Biologia, Kraków: Wydawnictwo Zielona Sowa, 2008, s. 116, ISBN 978-83-7435-692-3.
- ↑ John McMurry, Chemia organiczna, wyd. 3, t. 4, Warszawa: Wydawnictwo Naukowe PWN, 2005, s. 954–955, ISBN 83-01-14406-8.
- ↑ Utlenienie cukrów, [w:] Aleksander Kołodziejczyk, Naturalne związki organiczne, wyd. 2, Warszawa: Wydawnictwo Naukowe PWN, 2006, s. 250–253, ISBN 978-83-01-14316-9.
- ↑ Czym jest syrop glukozowy i z czego jest wytwarzany?, [w:] Food-Info.net [online], Wageningen University, Holandia [dostęp 2016-01-09].
- ↑ a b Glucose [online], Cosmetics Info [dostęp 2022-07-12] (ang.).
- ↑ Glucose, [w:] CosIng [online], European Commission [dostęp 2022-07-12] (ang.).
Bibliografia edytuj
- CRC Handbook of Chemistry and Physics, William M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, ISBN 978-1-4987-5429-3 (ang.).